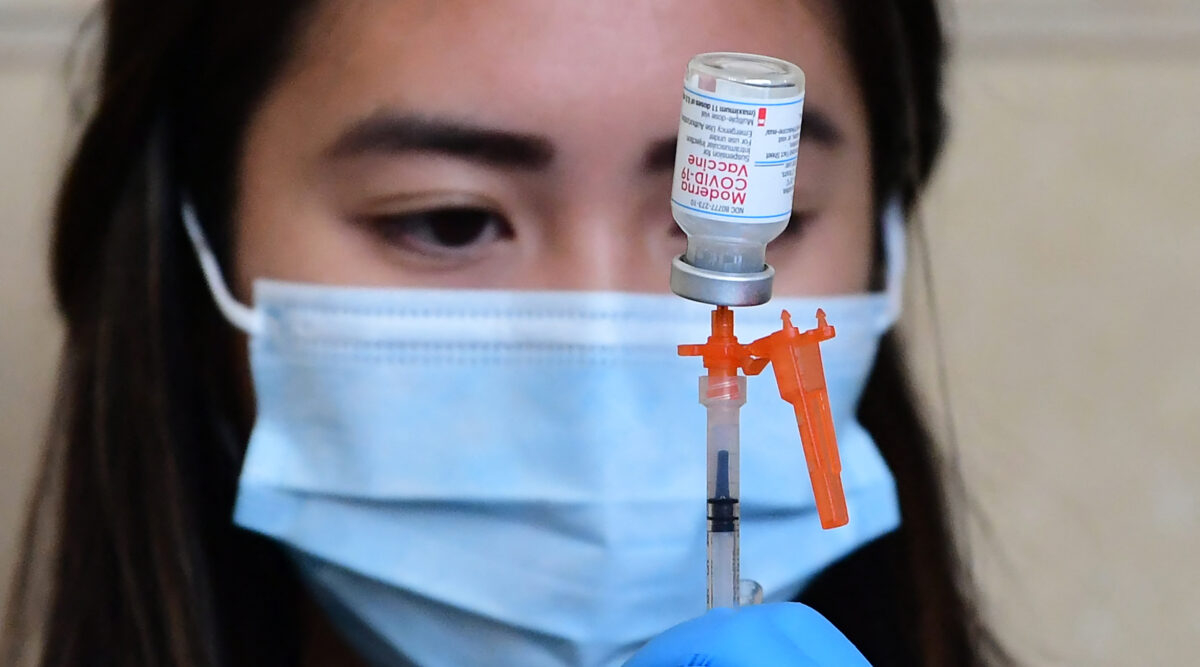
Cơ quan quản lý dược phẩm của Mỹ hiện đã cấp phép chính thức cho phiên bản vaccine COVID-19 tên Comirnaty của Pfizer, và Spikevax của Moderna, nhưng các phiên bản này chưa thấy có ở Mỹ. Những phiên bản vaccine đang có sẵn đều chưa được cấp phép chính thức, mà chỉ có giấy phép sử dụng khẩn cấp. Theo luật pháp Mỹ, người dân được lựa chọn từ chối hoặc chấp nhận dùng chế phẩm chưa được cấp phép chính thức.
Cơ quan Quản lý Thực phẩm và Dược phẩm của Mỹ (FDA) đã cấp phép chính thức cho Spikevax của Moderna vào 31/01/2022, sau khi đã cấp phép chính thức cho Comirnaty của Pfizer vào 23/08/2021.
Ngoài ra, FDA cũng cấp lại giấy phép sử dụng khẩn cấp cho phiên bản "Moderna COVID‑19 Vaccine" của Moderna cùng ngày 31/01. Tương tự, phiên bản "Pfizer-BioNTech COVID-19 Vaccine" của Pfizer cũng đã được cấp giấy phép sử dụng khẩn cấp lại nhiều lần.
Trong thư gửi Moderna thông báo cấp lại giấy phép sử dụng khẩn cấp cho phiên bản Moderna COVID‑19 Vaccine, FDA nói rằng, không có "đủ" nguồn cung cho cả 2 loại vaccine đã được cấp phép chính thức.
"Mặc dù Spikevax (COVID-19 Vaccine, mRNA) và Comirnaty (COVID-19 Vaccine, mRNA) đã được cấp phép chính thức để ngăn ngừa COVID-19 ở một số cá nhân — trong phạm vi được cấp phép sử dụng khẩn cấp của Moderna COVID-19 Vaccine, vẫn chưa có đủ vaccine đã được cấp phép chính thức để phân phối cho toàn dân" vào lúc ban hành giấy phép ngày 31/01.
Tờ Epoch Times cho biết, vào tháng 10/2021, Comirnaty đã không được phân phối ở Mỹ. Trong tuần này, tờ Epoch Times đã gửi câu hỏi đến các quan chức ở tất cả 50 tiểu bang tại Mỹ về phiên bản vaccine mang nhãn hiệu Comirnaty. 12 tiểu bang xác nhận rằng, họ vẫn chưa nhận được các lọ vaccine mang nhãn hiệu Comirnaty.
"Không có bang nào nhận được sản phẩm Comirnaty", một phát ngôn viên của Nội các Dịch vụ Gia đình và Sức khỏe của Khối thịnh vượng chung Kentucky cho biết trong email gửi tờ Epoch Times.
Đã có thời điểm, lọ Pfizer có nắp màu xám, sử dụng một chất đệm khác, "được kỳ vọng là sẽ có nhãn 'Comirnaty' trên đó, nhưng nó không có", phát ngôn viên của Bộ Y tế Bang Washington cho hay.
Bang Washington đã nhận được khoảng 235.000 liều chế phẩm nắp xám, và các bang khác cũng đã bắt đầu nhận sản phẩm có nắp xám ấy.
"CDC vẫn chưa bắt đầu phân phối sản phẩm mang nhãn hiệu Comirnaty", một phát ngôn viên của Bộ Y tế Utah cho hay trong email gửi tờ Epoch Times. Email này cũng cho biết thêm rằng "nhân viên chương trình tiêm chủng của chúng tôi chưa nghe được từ CDC về mốc thời gian cho sự thay đổi này".
CDC là từ viết tắt của Trung tâm Kiểm soát và Phòng ngừa Dịch bệnh.
Cơ quan này đã không trả lời các đề nghị bình luận về sự có mặt của Spikevax và Comirnaty trên thị trường.
CDC cho biết trên trang web của họ rằng, Pfizer "không có kế hoạch sản xuất" bất kỳ sản phẩm nào mang nhãn hiệu Comirnaty, vì sản phẩm mang giấy phép sử dụng khẩn cấp (EUA) vẫn đang có sẵn và đang được cung cấp. Trang web chưa được cập nhật sau khi Spikevax được cấp phép chính thức.
Khi được đề nghị đưa ra bình luận, FDA đã chỉ tờ Epoch Times đến các công ty vaccine. Nhưng các công ty này chưa cho biết khi nào các loại vaccine được cấp phép chính thức sẽ có mặt trên thị trường.
Một phát ngôn viên của Pfizer cho tờ Epoch Times biết vào năm ngoái rằng, Pfizer sẽ dùng sản phẩm mang giấy phép sử dụng khẩn cấp cho đến khi sản phẩm hết hạn.
Theo tổ chức hỗ trợ pháp lý Liberty Counsel, việc thiếu các loại vaccine đã được cấp phép chính thức là rất quan trọng, vì điều đó có nghĩa là mọi người vẫn có quyền chấp nhận hoặc từ chối các loại vaccine đang có mặt (chỉ có giấy phép sử dụng khẩn cấp).
"Hiện tại không có một loại vaccine COVID được FDA cấp phép đầy đủ nào mà có sẵn cho người dân. Cả Comirnaty và Spikevax đều không có sẵn. Mọi thứ đang có sẵn vẫn tuân theo luật sử dụng khẩn cấp. Điều đó có nghĩa là mọi người có tùy chọn chấp nhận hoặc từ chối các loại vaccine ấy", ông Matthew Staver, người sáng lập và chủ tịch của Liberty Counsel, tuyên bố.
Liberty Counsel đang đại diện cho các nguyên đơn trong nhiều vụ kiện không thừa nhận các lệnh bắt buộc tiêm chủng, bao gồm cả một vụ kiện quân đội Mỹ.
Tờ thông tin của FDA (pdf) cung cấp cho những người chuẩn bị tiêm chủng nói rằng, "theo giấy phép sử dụng khẩn cấp, việc tiêm hay không tiêm" vaccine là sự lựa chọn của bạn, dựa trên ngôn từ của Bộ luật Hoa Kỳ: Tiêu đề 21, 360bbb-3(e)(1)(A)(ii)(III).
Tuy nhiên, một số cho rằng, luật pháp Mỹ không cấm các quy định bắt buộc tiêm chủng.
Bộ Tư pháp Mỹ đã đưa ra một ý kiến pháp lý (pdf) vào năm ngoái rằng, luật pháp "không cấm các thực thể áp đặt các yêu cầu về tiêm chủng".
FDA cho biết, các phiên bản được cấp phép sử dụng khẩn cấp và cấp phép chính thức của vaccine là "khác biệt về mặt pháp lý, với một số khác biệt nhất định không ảnh hưởng đến độ an toàn hay hiệu quả". FDA đã từ chối đưa ra bình luận về tuyên bố này.
Moderna đã không trả lời đề nghị bình luận từ tờ Epoch Times. Pfizer thì cho biết, các sản phẩm "được tạo ra bằng các quy trình giống nhau và không có sự khác biệt giữa chúng về độ an toàn hay hiệu quả". Người phát ngôn của Pfizer cho biết thêm, câu "khác biệt về mặt pháp lý, với một số khác biệt nhất định không ảnh hưởng đến độ an toàn hay hiệu quả" nằm trong thư của FDA là đề cập đến "sự khác biệt về thông tin sản xuất trong các bản đệ trình theo quy định".
Cao Dương
Theo The Epoch Times
Xem thêm:
- Vaccine COVID-19 của Moderna được FDA Mỹ cấp phép chính thức: Ban tư vấn của CDC Mỹ sẽ họp
- Thụy Điển đình chỉ vaccine Moderna vô thời hạn do nguy cơ bệnh tim
- Cơ quan y tế Pháp khuyến nghị người dưới 30 tuổi không nên tiêm vaccine ngừa COVID-19 của Moderna
- Chủ tịch Moderna: Tất cả các vaccine có thể khó có hiệu quả với Omicron
- Báo động tình trạng ngăn chặn thông tin tác dụng phụ có hại của vaccine COVID-19